REVERSIBLE
Bonjour et bienvenue sur le site de l’association « Les Petits MecP2 ».
L’association française « Les petits Mecp2 » est dédiée aux familles touchées par le syndrome de duplication du gène MECP2, une anomalie génétique rare, progressive et grave. Nos missions visent à soutenir les familles, informer sur les avancées scientifiques, financer des projets de recherche et soutenir la mise en place des prochains essais cliniques en FRANCE.
Qu'est ce que le syndrome de duplication Mecp2 ?
Le syndrome de duplication du gène MECP2, ( en anglais : MDS, en français: Mecp2DupS ), est une maladie génétique rare touchant principalement les garçons.
La protéine codée par le gène MECP2, joue un rôle central dans la régulation d’autres protéines responsables du développement et du fonctionnement du cerveau.
La duplication du gène entraîne une surproduction de la protéine MeCP2 empêchant ainsi la régulation d’autres protéines. Ceci se traduit cliniquement notamment par une déficience intellectuelle (DI) modérée à sévère, un retard de développement psychomoteur, un langage très pauvre ou absent, des infections pulmonaires, de l’épilepsie…
En conséquence, la quantité de la protéine MeCP2 présente dans les tissus doit être régulée de façon précise : ni trop faible, ni trop élevée, pour assurer le bon fonctionnement du réseau neuronal.
Le syndrome de duplication du gène MECP2 étant très largement sous-diagnostiqué à cause de la variabilité des symptômes, la prévalence exacte du syndrome reste actuellement méconnue. On l’estime à ce jour à 1/150 000 naissances de garçon.
Actuellement, le nombre de cas dans le monde est inconnu. Cependant, il est possible que le syndrome de duplication du gène MECP2 puisse représenter 1 à 2% des déficiences intellectuelles inexpliquées et/ou de l’autisme.
C’est pourquoi il est primordial de répertorier tous les cas diagnostiqués au travers des registres déjà existants.
Les causes
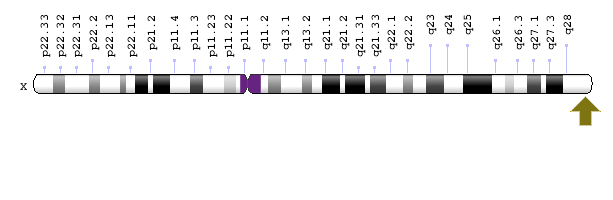
La duplication du gène MECP2 est causée par la duplication de l’ADN sur la région du chromosome Xq28 (28eme partie du bras long du chromosome X).
Ce n’est pas une maladie neurodégénérative inéluctable comme le syndrome de RETT.
Les problèmes d’occlusion sont dus à la duplication du gène voisin de MECP2 (FLNA – Filamine), un autre gène est également responsable de désordre : Irak1. Selon certaines études, ce gène serait responsable d’un déficit immunitaire et d’une grande fragilité pulmonaire.
La région Xq28 contient plusieurs gènes dont le MECP2 et IRAK1, GDI1, FLNA, L1CAM, IDH3G. Le début et la fin en double (points d’arrêt) varient entre les individus. La constatation est désormais établie que la duplication du gène MecP2 joue un rôle important dans les troubles du système nerveux. Des souris génétiquement modifiées avec 2 fois le niveau normal de la proteine MecP2, développent les caractéristiques du syndrome de duplication. Ces études démontrent bien que MecP2 (plutôt que d’autres proteines) est le coupable de cette anomalie. MecP2 a aussi un autre effet : Plus la proteïne est produite, moins les patients ressentent la douleur.
Certains enfants présentent également des anomalies (duplication) sur le chromosome Xq26.3 comprenant 23 gènes.
Dans plus de 90% des cas, la duplication est héritée d’une mère porteuse asymptomatique. On parle de porteur lorsque la personne est porteuse du défaut génétique, mais que celui-ci ne s’exprime pas cliniquement.
Lors d’une grossesse, la mère a 50% de risque de faire naître un garçon atteint et 50% de mettre au monde une fille porteuse de la mutation. Il est très rare que les filles développent une forme symptomatique de la maladie.
Les hommes (XY), ne possèdent qu’un seul chromosome X. La duplication du gène MECP2 cause dans tous les cas des symptômes graves.
Contrairement aux hommes, les femmes (XX) possèdent 2 chromosomes X. Une duplication du gène MECP2 a très rarement des conséquences sur une femme, car le chromosome X ayant du matériel dupliqué est inactivé et le taux de protéine MeCP2 reste normal.
Dans de rares cas, la mutation est exprimée chez les femmes à cause d’une inactivation défavorable du chromosome X muté, ou parce que la mutation est transposée sur un autre chromosome.
La duplication du gène MECP2 peut également apparaitre lors de la fécondation. On parle alors de mutation de novo car aucun des parents n’est porteur de la mutation génétique.
En terme d’espérance de vie, différentes études démontrent une mortalité importante vers la vingt-cinquième année. Ce n’est pas la duplication qui en est la cause mais les pathologies (infections respiratoires principalement) qui en sont responsables. Nous avons aussi rencontré des porteurs de l’anomalie de plus de 40 ans.
Les symptômes
Les principaux symptômes retrouvés chez les patients atteints du syndrome de duplication du gène MECP2 sont:
- Déficience intellectuelle (DI)
- Retard de développement
- Altération de la coordination motrice (ataxie)
- Absence de langage
- Manque de tonus musculaire (hypotonie) et spasticité progressive
- Epilepsie
- Infections récurrentes
- Réduction de la sensibilité à la douleur
- Troubles gastro-intestinaux (reflux ou constipation)
- Troubles buccaux dentaires
- Troubles ophtalmologiques et baisse de l’audition
- Traits autistiques
- Morbidité précoce
Les cas répertoriés de syndrome de duplication du gène MECP2 sont peu nombreux. Un enfant atteint du syndrome peut ne pas présenter tous les symptômes listés. De plus, les symptômes et leurs intensités peuvent évoluer avec l’âge.
Le diagnostic

Le diagnostic peut être évoqué à partir de l’examen clinique, chez un enfant de sexe masculin présentant un retard des acquisitions et/ou une déficience intellectuelle sévère avec stéréotypies associées à de l’épilepsie, des infections récurrentes pulmonaires ou ORL, une constipation chronique.
Le diagnostic clinique doit être confirmé par la recherche d’une duplication de la région Xq28 comportant le gène MECP2 après une évaluation dans un centre de référence ou de compétence des «déficiences intellectuelles de causes rares» ou des «Anomalies du développement et syndromes malformatifs». Avec la généralisation des technologies d’ACPA (puce à ADN), voire de séquençage haut débit d’exome, un diagnostic non guidé par la clinique – et donc plus précoce au cours de la vie – est de plus en plus fréquent.
La prise en charge thérapeutique est multidisciplinaire, symptomatique, et comprend des interventions souvent communes à d’autres polyhandicaps (rééducations pluridisciplinaires, appareillage, prise en charge nutritionnelle et respiratoire, soutien psychologique) et d’autres ciblant des besoins plus spécifiques du MECP2 (prise en charge des difficultés alimentaires initiales, traitement de l’épilepsie, de la constipation, des infections récurrentes).
Le tableau clinique est évolutif, justifiant une surveillance spécialisée tout au long de la vie.
Le suivi des patients atteints de MECP2 doit se faire au minimum annuellement et plus fréquemment si nécessaire selon l’âge et les complications associées, en collaboration avec un centre de référence ou de compétences disposant de l’ensemble des spécialistes nécessaires à une prise en charge multidisciplinaire du polyhandicap et de l’épilepsie.
La Réversibilité
Le professeur Zoghbi et son équipe ont rapporté le résultat de leur étude dans « Nature ». Ils ont montré que les symptômes sont réversibles chez les souris après un traitement avec des oligonucléotides antisens.
Les projets de recherche

- Les Oligonucléotides antisens, (Professeur Zoghbi, Houston Texas)
En collaboration avec la compagnie pharmaceutique IONIS Pharmaceutical, un groupe du Pr.Zoghbi, dirigé par Dr.Davut Pelhivan a développé un médicament potentiel faisant partie de la famille des « Antisens » (ASO). Cette molécule, en cours d’études cliniques, réduit spécifiquement le niveau de protéine MeCP2 dans les cellules du cerveau, notamment.
L’équipe de Zoghbi et Pelhivan a développé un modèle de souris dans lequel le sujet manifeste les symptômes typiques observés chez les enfants atteints du syndrome de duplication du gène MECP2.
En 2015, l’équipe a démontré qu’il est possible d’inverser les symptômes du syndrome sur ce modèle de souris. La normalisation de la concentration de la protéine MeCP2, après administration d‘ASO a permis l’amélioration de tous les symptômes caractéristiques du syndrome chez la souris, même en commençant le traitement à un âge avancé.
En 2021, afin de préparer des études cliniques, l’équipe du Pr.Zoghbi a créé un modèle de souris qui, comme les enfants atteint du syndrome de duplication du gène MECP2, possèdent 2 copies du gène MECP2 humain. Ce nouveau modèle de souris a permis de confirmer les résultats précédemment obtenus avec les ASO. Ces résultats donnent l’espoir de pouvoir inverser les symptômes également chez l’Homme. Pour cela, il est nécessaire de délivrer les ASO efficacement dans le cerveau et de contrôler, en toute sécurité, le niveau de la protéine MeCP2.
Les chercheurs travaillent actuellement sur une nouvelle méthode d’administration des ASO par injection intracérébroventriculaire permettant une distribution beaucoup plus large du médicament dans le cerveau. Cette technique s’est jusque-là avérée efficace chez les nourrissons humains atteints d’autres maladies.
Enfin, comme il est essentiel d’avoir un taux de protéine MeCP2 correct dans le cerveau, l’équipe doit déterminer avec précision la dose d’ASO nécessaire pour chaque patient. C’est pourquoi, les études cliniques suivantes sont en cours avant de pouvoir intervenir sur l’Homme:
-Evaluation des biomarqueurs : La protéine MeCP2 régule d’autres protéines qui elles-mêmes ont un effet sur l’organisme. La surdose de la protéine MeCP2 entraine une variation de ces protéines. En identifiant des biomarqueurs/protéines qui sont régulés par la protéine MeCP2, les chercheurs pourront rapidement évaluer l’efficacité de l’ASO administré.
– Sévérité clinique : établir un lien entre le type de duplication et les symptômes qui en découle au cours du temps afin d’évaluer l´efficacité du traitement par rapport aux symptômes du patient.
– Etudes génétiques : permettre de déterminer avec précision les types de duplication et adapter le dosage d’ASO à chaque individu.
- Le repositionnement de Médicaments, (Docteur Prehivan, Houston, Texas)
L’objectif de ce projet est de trouver un médicament, déjà sur le marché, capable de réduire le niveau de cette protéine. Deux approches sont utilisées :
– Tester un maximum de médicaments actuellement approuvé par la FDA (Agence américaine du médicament) sur d’autres cibles thérapeutiques afin de voir s’ils ont un effet sur la protéine MeCP2 (ex : dégradation, inactivation etc..). L’avantage de cette méthode est que le développement clinique du médicament est grandement accéléré, puisque son profil de sécurité est validé.
– Tester chaque gène du génome pour identifier ceux qui régulent l’expression de la protéine MeCP2. Une fois ces régulateurs identifiés, les chercheurs s’efforceront de trouver des médicaments, déjà sur le marché, pour les inhiber. Plusieurs régulateurs du gène MECP2 ont déjà été identifiés. Un médicament ayant une action sur l’un de ces régulateurs a déjà permis d’améliorer certains symptômes chez la souris porteuse de la duplication du gène MECP2.
L´équipe du Dr.Pehlivan poursuit la recherche sur l’identification de nouveaux régulateurs et l’évaluation des médicaments afin de trouver ceux qui offriront la plus grande efficacité tout en limitant les possibles effets secondaires.
- Les ARN Interférants, (Professeur Khvorova, Boston Massachusetts)
Pr. Anastasia Khvorova est une pionnière dans le domaine des oligonucléotides et fait partie de l’UMASS à Boston (Massachusetts) qui regroupe de nombreux experts en ARN, notamment le lauréat du Prix Nobel de médecine 2006 Craig Mello.
L’équipe du Pr. Khvorova a utilisé de petits oligonucléotides interférant avec l’ARN (SiRNA) afin d’empêcher la traduction des protéines ciblées en se liant à leur ARN messager et en favorisant sa dégradation. Des ciseaux moléculaires sont guidés par le SiRNA vers l’ARN messager MeCP2 pour le détruire, réduisant ainsi le niveau de protéine MeCP2 dans la cellule.
Le modèle développé par Pr.Khvorova montre une distribution robuste de SiRNA dans tout le cerveau et la moelle épinière. Son approche suggère qu’un traitement pourrait être administré une fois par année, afin de garder le taux de la protéine MeCP2 à un niveau constant.
- CRISPR, CAS, (Docteur Cohn, Toronto, Canada)
Dr. Cohn et son équipe proposent une stratégie de modification du génome. Ce projet utilise la technique d´édition du génome connue sous le nom de CRISR-CAS9, qui a valu le Prix Nobel de Chimie 2020 à Emmanuelle Charpentier et Jennifer Doudna.
Cette technique consiste à « corriger » directement l’ADN, conduisant dans les cas de duplication du gène MECP2, à supprimer définitivement et spécifiquement la zone dupliquée. Une seule copie du gène MECP2 subsiste alors dans chacune des cellules visées, ce qui a pour conséquence la normalisation de la concentration de protéine MeCP2.
Un modèle de souris pour tester cette stratégie thérapeutique a déjà été développé et est prête à être utilisée. Le Dr. Cohn et son équipe ont déjà démontré que cette technique fonctionne sur les fibroblastes (cellules de la peau) de patients atteints du syndrome de duplication du gène MECP2.
En utilisant la même approche, le groupe de chercheurs a également observé une amélioration des symptômes dans un modèle de souris ayant développé la dystrophie musculaire de Duchenne.
La voie d’administration de ce type de nouveau traitement est en cours d‘évaluation.
- Les registres (base de données internationale de collecte d’informations médicales)
La recherche clinique a besoin de connaître les patients atteints par la duplication pour recueillir le plus d’informations possible sur cette maladie rare et renforcer les connaissances sur le syndrome. Il existe plusieurs registres sur lesquels les enfants porteurs de la duplication peuvent être enregistrés :
-Le registre de l’institut de recherche neurologique : en savoir plus
-Le registre Genida : en savoir plus
Vous êtes disposé à fournir et mettre à jour des informations médicales qui seront anonymisées et qui permettront de faire progresser la connaissance sur la maladie génétique qui touche votre enfant, frère, sœur ou proche.
En vous inscrivant, vous aiderez la recherche sur le syndrome de la duplication MecP2 !
